|
|
Órgão Oficial de Divulgação Científica da
|
ISSN: 1679-1796
|
Nefrectomia Parcial Videolaparoscópica: Modelo Experimental em Ratos
Laparoscopic Partial Nefrectomy: An Experimental Model in Rats
Fernando Meyer, Sérgio Ossamu Ioshii, Andressa Hubar Patriani, Bruno de Figueiredo Pimpão, Ruy Fernando Kuenzer Caetano da Silva
Hospital Universitário Cajuru da Pontifícia Universidade Católica do Paraná (PUCPR)
A nefrectomia parcial é um procedimento utilizado em pacientes com doença localizada e com indicação de
preservação da função renal. Atualmente, a indicação mais freqüente tem sido para tratamento dos tumores renais
localizados, principalmente os menores de 4 cm, de pólo inferior e exofíticos. OBJETIVO: Estabelecer um modelo experimental de
nefrectomia parcial laparoscópica em ratos. MÉTODOS: Foram utilizados 40 ratos Rattus Norvegicus albinus da linhagem Wistar, machos, com
peso maior do que 350 gramas. A anestesia foi obtida através da administração intraperitoneal de Tiopental 65 mg/kg. Logo em seguida
os animais foram submetidos à insuflação através da agulha de Veress com
PCO2 de 5 mmHg. Após o pneumoperitônio foram
introduzidos três trocartes de 5 mm, dois sobre a linha mediana e outro no quadrante inferior esquerdo. Para a ressecção do pólo renal inferior,
no grupo A foi utilizado o bisturi elétrico conectado à tesoura e no grupo B, o bisturi harmônico. Todos os animais foram mortos após
o término dos experimentos. RESULTADOS: Não houve complicações graves no trans-operatório ou necessidade de conversão
para nefrectomia aberta. No grupo A o tempo operatório médio foi de 50,80 +/_ 4,72s e no grupo B foi de 84,95 +/_ 5,16s
(p<0,0001). CONCLUSÃO: Neste modelo, o material cirúrgico é o mesmo utilizado em humanos e são aplicados todos os procedimentos básicos
da cirurgia laparoscópica, tornando-o factível para o treinamento de acadêmicos, médicos, residentes e cirurgiões.
Palavras-chave: NEFRECTOMIA PARCIAL, LAPAROSCOPIA, VIDEOLAPAROSCOPIA EM RATOS
PURPOSE: To describe a model of laparoscopic partial nefrectomy in rats. METHODS: 40 males rats
Rattus Norvegicus albinus Wistar, aged 20 weeks, weighting more than 350g, were used in this study. The animals
were divided in 2 groups: group 1 where an eletric scalpel was used to do the partial nefrectomy and group 2 an harmonic scalpel was
used. They were anesthetized with Tiopental 65mg/kg intraperitoneum and insufflated with
PCO2 of 5mmHg trough a Veress needle.
After the pneumoperitoneum, three 5 mm trocar were passed trough the abdominal wall, two in the medium abdominal line and one in
the left lower square. The ressection of the inferior renal segment performed in the group 1 using the eletric scalpel and in the group
2 using the harmonic scalpel. The animals were sacrificed in the end of the experiments. RESULTS: All rats survived until the end of
the surgery. In the first group the average lenght of the surgery was
50,80+-4,72s and in the second group
84,95+-5,16s (p<0,0001).
In relation to complications, nothing serious was observed and no conversion to open surgery was necessary. CONCLUSIONS: In
this model, the material is the same used in human surgeries with all laparoscopic procedure, becoming doable for surgeon',
residents' and students's training and improvement.
Key words: partial nephrectomy, laparoscopic, rats.
|
MEYER F, IOSHII SO, PATRIANI AH, PIMPÃO BF, DA SILVA RFKC Nefrectomia Parcial Videolaparoscópica: Modelo Experimental em Ratos. Rev bras videocir 2005;3(4): 183-190. |
||
|
Recebido em 03/11/2005 |
|
Aceito em 15/11/2005 |
|
|
nefrectomia parcial é um procedimento urológico utilizado em
pacientes selecionados, isto é, com doença localizada e
com indicação de preservação da função
renal. Urolitíase, carcinoma de células renais
(CCR), trauma, duplicidade de via excretora e
hipertensão arterial secundária a segmento isquêmico estão
entre as condições mais aceitas para a realização
desta técnica 1,2,3. Atualmente a indicação mais
freqüente tem sido para tratamento dos tumores
renais localizados. Devido à ampla utilização da
ultra-sonografia abdominal e da tomografia
computadorizada para avaliação das doenças
intra-abdominais e retroperitoneais, houve aumento na incidência
da detecção incidental de massas renais
assintomáticas 4,5. Embora essas lesões sejam pequenas e de
baixo estadio, a maioria tende a ser maligna
6,7,8.
Embora a nefrectomia laparoscópica (NL) já esteja bem estabelecida e aceita pela
comunidade urológica, desde a descrição do primeiro caso
por R. Clayman em 19919. A nefrectomia
parcial laparoscópica (NPL) não tem obtido a
mesma popularidade devido aos problemas associados
com a hemostasia do parênquima renal e ao risco
de fístula urinária 9. A NPL foi inicialmente
descrita em modelo animal 10 e subseqüentemente
realizada no ser humano, por via transperitoneal
5 e retroperitoneal 11. Devido aos relatos iniciais de
altas taxas de complicações e de conversão para
cirurgia aberta, vários pesquisadores têm
desenvolvido técnicas para facilitar o procedimento,
melhorando a hemostasia e diminuindo a morbidade
operatória 12,13,14.
Revisando-se as várias técnicas
laparoscópicas, observa-se que não há consenso quanto
ao melhor método para se obter a hemostasia.
Assim sendo, ocorre ao contrário do procedimento por
via aberta, onde o clampeamento do hilo renal, a hipotermia in situ, a ligadura dos vasos bem como
a sutura do sistema coletor fazem parte do
protocolo padrão. Esses princípios têm sido evitados
nos procedimentos laparoscópicos devido à
dificuldade em se realizar essas manobras laparoscopicamente
15,16.
Tendo conhecimento da dificuldade
técnica na realização da NPL e da incidência de
complicações, este estudo experimental tem como objetivo
evidenciar uma técnica de treinamento para cirurgiões.
MÉTODOS
O projeto experimental executado foi desenvolvido e aprovado na Comissão de Ética
de nossa instituição segundo os princípios do
Colégio Brasileiro de Experimentação Animal
(COBEA, 1999).
Na realização deste projeto de
pesquisa foram utilizados 40 ratos machos, da linhagem
Wistar (Norvergicus albinus)
Todos os animais apresentavam-se com 20 semanas de idade, peso maior que 350
gramas, apresentando bom aspecto geral, ativos e
sem evidência de doença à inspeção. Foram
excluídos do estudo os animais que foram a óbito durante
a indução anestésica.
Os animais, após permanecerem sob condições de laboratório padronizadas
(temperatura entre 20 e 24°C, umidade relativa entre 50 e
60%, sob condições controladas de luz - ciclo
dia/noite de 12 horas [8:00 _ 20:00], recebendo ração
para ratos (NUVILAB-CR1, Nuvital, Curitiba) e
água ad libitum, foram mantidos em jejum por oito
horas antes do procedimento. O experimento foi
conduzido segundo os princípios éticos da
experimentação animal 17.
Esta pesquisa consistiu, basicamente, em realizar-se um modelo de nefrectomia
parcial laparoscópica em ratos, utilizando-se para tal,
bisturi elétrico ou bisturi harmônico. Em razão
da característica do experimento, os animais
foram distribuídos de forma aleatória em dois
lotes, designados de Grupo A e Grupo B.
Grupo A: Constituído de 20 animais os quais
foram submetidos a NPL do lado esquerdo,
utilizando-se bisturi elétrico.
Grupo B: Constituído de 20 animais os quais
foram submetidos a NPL do lado esquerdo,
utilizando-se bisturi harmônico.
Equipamento e Instrumental
Para o procedimento laparoscópico foram utilizados os seguintes materiais:
1. Sistema de vídeo com microcâmera Storz®
Dx-cam ntsc (202301 20)
2. Insuflador de CO2 automático Storz
3. Fonte de luz (Xenon)
4. Agulha de Veress
5. Trocartes Endopath com ponta dilatadora 5
mm (75 mm) (Ethicon Endo-Surgery)
6. Ótica Storz® Hopkins II de 0° para
cistoscopia (27005-AA)
7. Pinça laparoscópica de preensão 5 mm
8. Pinça laparoscópica de dissecção 5 mm
9. Tesoura laparoscópica 5 mm
10. Bisturi elétrico (Electrosurgical Generator
SS-200 WEM)
11. Bisturi Harmônico (Harmonic Scalpel
- Ultracision® - Endo-Surgery)
12. Tesoura coaguladora curva (CS-23C) de 23
cm X 5 mm (Endo-Surgery)
TÉCNICA OPERATÓRIA
Indução Anestésica
A indução anestésica foi obtida através
da injeção intraperitonial de Tiopental, na dose de
65 mg/Kg. O controle da sedação foi
efetuado avaliando-se o reflexo de retirada da pata do
animal ao estímulo doloroso. Quando
necessário, administrou-se uma segunda dose de anestésico
18.
Após indução anestésica, os animais
foram pesados em balança eletrônica de alta
precisão (marca Ohaus® Precision Standard modelo
TS-2KS).
Ato Operatório
Os animais foram posicionados em
decúbito dorsal, numa prancha de cortiça, com os
quatro membros fixados a mesa cirúrgica. Foi
realizada tricotomia ampla da face ventral do rato,
seguida de anti-sepsia cuidadosa.
Realizou-se o pneumoperitônio com agulha de Veress posicionada na linha média do
abdômen, a dois terços abaixo do processo xifóide, através
de incisão de 5 mm na pele (Figura-1). Para executar
a punção com a agulha, foi necessária a tração
manual da parede abdominal anterior do rato para
sua realização com segurança, sem lesão de
estruturas intra-peritoneais. Procedeu-se à insuflação
da cavidade com CO2, até se atingir a pressão
máxima de 5 mmHg (3-5 mmHg)18,19. Após a retirada
da agulha, divulsionou-se a pele com pinça hemostática e inseriu-se o trocarte de 5 mm,
através do qual foi introduzida a óptica de 0°. Sob
visão, foram realizadas outras duas incisões de 5 mm,
a primeira em quadrante abdominal inferior
esquerdo e a segunda na linha média do abdômen (entre
o processo xifóide e o trocarte da óptica), onde
foram introduzidos os trocartes (5 mm) para as pinças
de preensão, dissecção e bisturi tanto elétrico
como harmônico (Figura-2). A passagem destes
trocartes também foi precedida da tração manual da
parede abdominal anterior do rato.
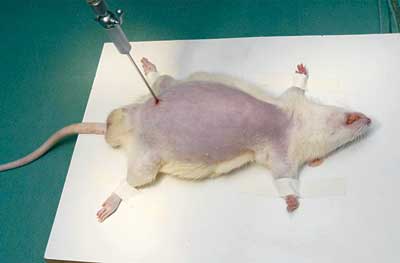 |
| Figura 1 - Agulha de veress e pneumoperitônio instalados. |
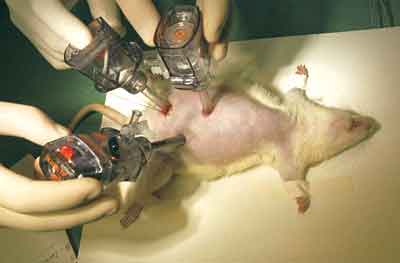 |
| Figura 2 - Posicionamento e fixação dos trocartes. |
Todos os trocartes foram fixados à pele
com fio mononylon 2-0, para impedir a
introdução exagerada ou a saída dos mesmos durante
o manuseio das pinças, evitando-se a perda
do pneumoperitônio19,20.
Após essa etapa, a mesa cirúrgica foi
elevada em 45° no lado esquerdo (Figura-3). Desta
maneira permitiu-se melhor visualização e exposição do
rim esquerdo para posterior realização da
nefrectomia parcial.
 |
| Figura 3 - Mesa cirúrgica com rotação lateral de 45 graus |
A seguir do posicionamento dos trocartes, realizou-se a inspeção da cavidade abdominal.
O cólon, o qual no rato não está fixado à
parede posterior, e o intestino delgado, foram
tracionados inferior e medialmente. Procedeu-se então
ao descolamento do rim esquerdo, liberando-o da gordura retroperitonial utilizando pinça de
preensão e tesoura.
Após completa mobilização do órgão,
o ureter foi identificado. Com o rim seguro por
meio de pinça de preensão posicionada ao seu
terço médio, iniciou-se a ressecção do pólo renal
inferior. (Figura-4).
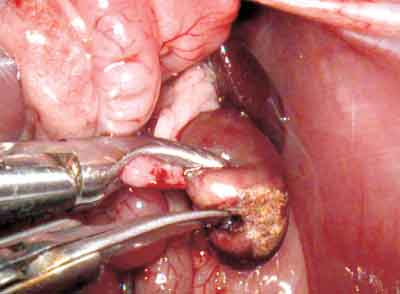 |
| Figura 4 - Imagem da cavidade abdominal mostrando a secção do pólo renal inferior |
Nos animais do Grupo A foi utilizado o bisturi elétrico conectado à tesoura,
mantendo-se a coagulação no nível 5 (0-10) do aparelho.
Nos animais do Grupo B foi utilizado o bisturi harmônico mantendo-o no nível 2 (função
VAR), com a lâmina cortante.
Após o término da nefrectomia parcial,
fez-se revisão da hemostasia e retirada dos trocartes
sob visão. Foi, então, desfeito o pneumoperitônio
e realizada sutura dos portais com fio mononylon 3-0.
Todos os animais foram mortos (dose letal de Tiopental 100 mg/Kg, intra-peritonialmente)
após a conclusão dos experimentos.
Tempo Operatório
O tempo despendido para realização
da nefrectomia parcial propriamente dita (tempo de secção), foi cronometrado nos dois grupos (A e
B). Iniciou-se a marcação do tempo com o início
da ressecção do pólo renal inferior e encerrou-se
com o término da hemostasia da mesma
14.
Em relação ao tempo de secção, testou-se
a hipótese nula de que o tempo médio quando
a operação é realizada com bisturi elétrico é igual
ao tempo médio quando a operação é realizada
com bisturi harmônico, versus a hipótese alternativa
de tempos médios diferentes.
RESULTADOS
Não houve complicações graves no
trans-operatório ou necessidade de conversão
para nefrectomia aberta.
Os animais do Grupo A tiveram peso médio de 397,10 ±17,13 g e os do Grupo B peso médio
de 396,80 ±14,67 g, evidenciando homogeneidade
dos pesos dos animais nos dois experimentos.
Nos 20 animais do Grupo A (bisturi
elétrico), o tempo operatório médio foi de 50,80 ± 4,72s e
nos 20 animais do Grupo B (bisturi harmônico) foi
de 84,95 ± 5,16s. O resultado do teste
estatístico indicou a rejeição da hipótese nula no nível
de significância de 5% (p<0,0001), (Gráfico-1).
Desta forma, pode-se dizer que há diferença
significativa entre as duas técnicas em relação ao tempo
de secção, sendo o procedimento com bisturi
elétrico realizado em menor tempo do que com o
bisturi harmônico.
O sangramento transoperatório foi desprezível e em nenhum dos animais
dos experimentos houve formação de fístula
urinária.
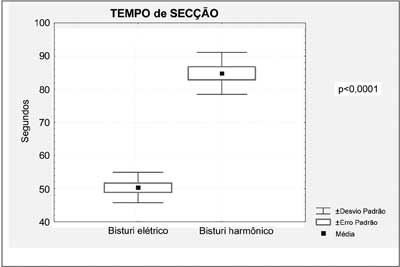 |
| Gráfico 1 - Tempo de secção (s) nos animais do experimento I (bisturi elétrico) e do experimento II (bisturi harmônico) |
DISCUSSÃO
A vídeo-laparoscopia é técnica
cirúrgica consagrada, e o sucesso deste procedimento
pode ser atribuído à redução da dor pós-operatória, à
curta permanência hospitalar e ao rápido retorno
às atividades normais. Entretanto o aprendizado
deste método para posterior aplicação na prática
clínica requer treinamento intensivo, com utilização
de tecidos inertes, simuladores e animais de
cirurgia experimental 18.
Animais de médio e grande porte, como cães e porcos, são utilizados em muitos modelos
de videolaparoscopia experimental, sendo bem
aceitos devido não só à semelhança da sua anatomia com
a do ser humano, como também à facilidade
técnica proporcionada por seu tamanho e à possibilidade
de se aproveitar em pacientes o instrumental
usado20. Entretanto, além de serem elevados os custos
para sua aquisição e manutenção, sabe-se pouco sobre
a fisiologia desses animais quando comparados a
outros modelos21. A restrição da legislação e a
opinião pública também têm dificultado o emprego
de grandes animais como modelo experimental.
Pequenos animais têm sido utilizados como modelo em cirurgia vídeo-laparoscópica.
O camundongo tem sido usado em laparoscopia como modelo para avaliar os efeitos do
pneumoperitônio sobre o estado imunológico e a biologia
tumoral, porém sua cavidade abdominal é muito pequena
para procedimentos laparoscópicos
complexos22.
O rato, apesar de suas diferenças com a anatomia humana, provou ser um valioso animal
para treinamento, pois dissecção, apreensão de
órgãos intra-abdominais, coagulação e sutura
intracorpórea podem neles ser
praticadas19. Além de tratar-se
de animal de baixo custo e amplamente estudado
19,22.
FILMAR e cols. (1987) relataram o primeiro experimento em que se utilizou a laparoscopia
em ratos. Os autores compararam a ocorrência
de aderência após lesão uterina ocasionada por
via laparoscópica e por laparotomia, não
encontrando diferença estatisticamente
significativa23. Apesar de não ser motivo de avaliação no presente
estudo, foram observadas aderências peritoneais
mais extensas nos ratos submetidos à secção com
bisturi elétrico. Esses achados deverão ser motivo de
estudos adicionais.
BERGUER et al. (1993), descrevendo um modelo de cirurgia laparoscópica em ratos na
qual realizaram fundoplicatura gástrica com
sucesso, demonstraram ser possível fazer
procedimentos complexos nesses pequenos
animais24.
Diversas técnicas já foram descritas em
ratos (fundoplicatura, esplenectomia, nefrectomia
total, ressecção hepática, herniorrafia,
colostomia, colectomia e exploração retroperitoneal). Para
tanto, diversos equipamentos endoscópicos e microcirúrgicos são necessários para
estes procedimentos (artroscópios, broncoscópios,
trocartes e pinças de 2 e 3 mm), o que restringe sua
aplicação. Quando acessível, entretanto, o uso de tal
material deve ser utilizado, pois permite maior espaço
de trabalho e treinamento de técnicas como sutura
livre em animais de pequeno porte, desenvolvendo a motricidade fina, enquanto preserva a
familiarização e aprendizado dos princípios básicos
da laparoscopia18. No presente estudo,
utilizamos trocartes de 5 mm em todos os portais, inclusive
o do bisturi harmônico, e a ótica utilizada foi a
do cistoscópio. Não encontramos dificuldade
técnica durante as punções e durante o manuseio
dos instrumentos, sendo a visualização do
campo operatório de boa qualidade. Porém, verificamos
que a fixação dos trocartes à pele do rato foi
fundamental para a realização do procedimento
proposto, mantendo-os estáveis e evitando a perda
do pneumoperitônio.
Devido à facilidade de obtenção e
manuseio do rato, e considerando a literatura aqui apresentada, optamos pela utilização deste
animal em nosso estudo, o qual confirmou a sua aplicabilidade na realização da NPL experimental.
Durante o projeto piloto pudemos observar que os animais com peso inferior a 350
gramas apresentavam maior dificuldade para a
realização do procedimento. Isto pôde ser notado durante
a colocação dos trocartes e também durante
a manipulação intra-abdominal, dificultando
a manutenção do pneumoperitônio e a realização
da operação proposta. Portanto, em nosso
trabalho utilizamos somente ratos com peso superior a
350 gramas.
A análise termográfica tem
demonstrado que o bisturi harmônico não aquece o tecido
acima de 80°C, entretanto requer maior tempo de
contato com o tecido que o bisturi elétrico. Isto pôde
ser confirmado neste trabalho, em que se analisou
o tempo decorrido desde o início da ressecção do
pólo renal até o seu término (tempo de secção).
Nos animais em que se usou o bisturi elétrico para
a realização da NPL o tempo médio foi de
50,30 segundos (±4,57); já naqueles em que foi usado
o bisturi harmônico o tempo médio foi de
84,80 segundos (±6,29), diferença essa
estatisticamente significativa (p<0,0001).
No estudo de ELASHRY et al. (1997), em que foi realizada NPL em modelo
experimental (porco), foram usados dois tipos de dissectores
ultra-sônicos (CUSA® e bisturi harmônico) e um tipo
de eletrodo eletrocirúrgico (ESE, Cook Urological
Inc., Spencer, IN). Os autores demonstraram que o
tempo para realizar a NPL foi significativamente
menor (p<0,0001) com o eletrodo eletrocirúrgico
(média 0,7 min) do que com os dissectores
ultra-sônicos (média 13,5 min)
13.
BARRET et al. (2001) realizaram NPL em porcos empregando três técnicas diferentes
de hemostasia do parênquima: bisturi
elétrico monopolar, bisturi elétrico bipolar e
bisturi harmônico. Os autores constataram que com o
bisturi harmônico é necessário um período mais
prolongado de contato com o tecido para sua secção e para
obter hemostasia25.
CONCLUSÕES
O modelo experimental apresentado neste trabalho mostra-se eficaz para que se proceda
a nefrectomia parcial laparoscópica em ratos
Wistar com o objetivo de treinamento de
acadêmicos, médicos residentes e até mesmo cirurgiões
nesta crescente área que é aplicação de
procedimentos minimamente invasivos no ato operatório.
Com uma técnica cirúrgica
devidamente padronizada, o rato é um modelo simples, barato
e eficaz.
O uso do bisturi elétrico, quando
comparado ao bisturi hamônico, se mostrou mais rápido
na realização da nefrectomia parcial.
Referências Bibliográficas
1. Walther MM, Choyke PL, Weiss G, Manolatos C, Long
J, Reiter R, Alexander RB, Linehan WM. Parenchymal sparing surgery in patients with hereditary renal
cell carcinoma. J Urol 1995; 153: 913-16.
2. Stifelman MD, Sosa RE, Nakada SY, Shichman SJ.
Hand-Assisted Laparoscopic Partial Nephrectomy. J
Endourol 2001;15 (2): 161-64.
3. Tash JA, Stock JA, Hanna MK. The role of
partial nephrectomy in the treatment of pediatric
renal hypertension. J Urol 2003; 169: 625-28.
4. Kozlowski PM, Winfield HN. Laparoscopic partial
nephrectomy and wedge resection for the treatment of
renal malignancy. J Endourol 2001; 15 (4): 369-74.
5. Winfield HN, Donovan JF, Lund GO, Kreder KJ,
Stanley KE, Brown BP, Loening AS, Clayman RV.
Laparoscopic Partial Nephrectomy: initial experience and
comparison to the open surgical approach. J Urol 1995;
153: 1409-14.
6. Polascik TJ, Pound CR, Meng MV, Partin AW,
Marshall FF. Partial nephrectomy: technique, complications
and pathological findings. J Urol 1995; 154: 1312-18.
7. Jeschke K, Peschel R, Wakonig J, Schellander L,
Bartsch G, Henning K. Laparoscopic nephron-sparing surgery
for renal tumors. Urology 2001; 58: 688-92.
8. Dall'Oglio MF, Srougi M, Gonçalves PD, Leite KM,
Hering F. Características morfológicas dos carcinomas de
células renais incidentais. Braz J Urol 2002; 28 (2): XVI-XXII.
9. Clayman RV, Kavoussi LR, Soper NJ, Dierks SM,
Meretyk S, Darcy MD, Roemer FD, Pingleton ED, Thomson
PG, Long SR. Laparoscopic nephrectomy: initial case
report. J Urol 1991; 146: 278-82.
10. Mc Dougall EM, Clayman RV, Chandhoke PS, Kerbl
K, Stone AM, Wick MR, Hicks M, Figenshau RS. Laparoscopic partial nephrectomy in the pig model. J
Urol 1993; 149: 1633-36.
11. Gill IS, Delworth MG, Munch LC. Laparoscopic
Retroperitoneal Partial Nephrectomy. J Urol 1994; 152:
1539-42.
12. Loughlin KR, Maranche J, Steele G, Dahl D, Comiter
C. Application of the harmonic scalpel to perform
partial nephrectomies in a porcine model. J Urol
1997; 157: 419A.
13. Elashry OM, Wolf Jr JS, Rayala HJ, McDougall
EM, Clayman RV. Recent advances in laparoscopic
partial nephrectomy: comparative study of electrosurgical
snare electrode and ultrasound dissection. J Endourol
1997; 11(1): 15-22.
14. Jackman SV, Cadeddu JA, Chen RN, Micali S,
Bishoff JT, Lee B, Moore RG, Kavoussi LR. Utility of the
harmonic scalpel for the laparoscopic partial nephrectomy.
J Endourol 1998; 12 (5): 441-44.
15. Ogan K, Cadeddu JA. Laparoscopic partial
nephrectomy: a procedure in evolution. Braz J Urol 2002; 28 (3): 1-9.
16. Cadeddu JA. Laparoscopic partial nephrectomy:
alternative approach to the small renal mass. AUA
News 2002; 6: 13.
17. Pereira CEM, Silva JDOM, Romero VR. Aspectos
Éticos da Experimentação Animal. Acta Cir Br 1998; 13
(2): 123-128.
18. Galesso MP, Cuck G, Pagan MR, Fernandes RC,
Perez MOC, Botter FCS. Orquiectomia laparoscópica:
modelo experimental em ratos. Braz J Urol 2002; 28 (2):
LVIII-LXI.
19. Giuffrida MC, Marquet RL, Kazemier G, Wittich
Ph, Bouvy ND, Bruining HA, Bonjer HJ. Laparoscopic
splenectomy and nephrectomy in a rat model: description
of a new technique. Surg Endosc 1997; 11: 491-4.
20. Sandoval BA, Sulaiman TT, Robinson AV, Stellato
TA. Laparoscopic surgery in a small animal model: a
simplified thecnique of retroperitoneal dissection in the
rat. Surg Endosc 1996; 10 : 925-27.
21. Bouvy ND, Marquet RL, Hamming JF, Jeekel J,
Bonjer HJ. Laparoscopic surgery in the rat: beneficial effect
on body weight and tumor take. Surg. Endosc., New
York, v. 10, p. 490-494, 1996.
22. Kaouk JH, Gill IS, Meraney AM, Desai MM,
Carvalhal EF, Fergany AF, Sung GT. Retroperitoneal minilaparoscopic nephrectomy in the rat model.
Urology 2000; 56 (6): 1058-62.
23. Filmar S, Gomel V, McComb PF. Operative
laparoscopy versus open abdominal surgery: a comparative study
on postoperative adhesion formation in the rat model.
Fertil Steril 1987; 48(3): 486-9.
24. Berguer R, Gutt C, Stiegmann GV. Laparoscopic
surgery in the rat: description of a new technique. Surg
Endosc 1993; 7: 345-7.
25. Barret E, Guilloneau B, Cathelineau X, Validire
P, Vallancien G. Laparoscopic partial nephrectomy in
the pig: comparison of the three hemostasis techniques.
J Endourol 2001; 15(3): 307-12.
ENDEREÇO PARA CORRESPONDÊNCIA
Fernando Meyer
Av Batel,1230 7º andar- Cj 703 Edifício Batel Trade Center
CEP 80420-907- Curitiba- PR- Brasil
Phone/Fax: (41) 3015-0303
E-mail: fmeyer@onda.com.br
